| Skrevet av Jens Lund - Professionsbachelor i Ernæring og Sundhed, BSc (Biokemi) BCAA er den engelske forkortelsen for Branched-Chain Amino Acids. På norsk heter det ”forgrenede aminosyrer”, og navnet henviser til den forgrenede sidekjeden som leucin, isoleucin og valin har. Det er altså disse 3 aminosyrene som utgjør BCAA, og som i løpet av for de siste par årene er blitt utrolig populære å benytte som kosttilskudd i forbindelse med trening. Men hvilken fysiologisk funksjon har BCAA, og er det overhodet nødvendig å supplere kostholdet sitt med disse aminosyrene? Det skal vi se nærmere på i denne artikkelen. 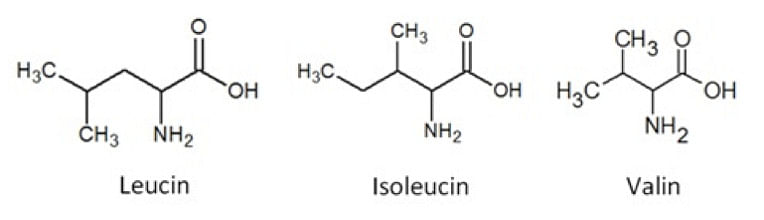  BCAA regulerer nemlig selve proteindannelsen" BCAA regulerer nemlig selve proteindannelsen" BCAA – Anabole og anti-katabole effekter Aminosyrer er byggesteinene som kroppens celler bruker når de skal produsere nye proteiner. Dette kan for eksempel være hormoner, enzymer, transportproteiner eller strukturproteiner. Vekttrening stimulerer muskelcellene til å produsere strukturproteinene aktin og myosin, som ivaretar musklenes sammentrekning. For at produksjonen av muskelproteiner kan forløpe optimalt, må musklene ha adgang til alle de nødvendige byggesteinene, dvs. de essensielle aminosyrene som kroppen ikke selv er i stand til å danne ut fra andre stoffer. Leucin, isoleucin og valin er slike essensielle aminosyrer, men BCAA fungerer også som mer enn bare byggeklosser. BCAA regulerer nemlig selve proteindannelsen. Det gjør de ved både å stimulere produksjonen og ved å hemme nedbrytningen av muskelproteiner (1 - 11).
 BCAA og muskelvekst Der er ingen tvil om at BCAA er viktig i forbindelse med muskelvekst. Vi må bare huske at leucin, isoleucin og valin også finnes i vanlige proteinrike matvarer, og det i gode mengder (12). Vanlig myseprotein er også rik på BCAA, så hvis man allerede spiser proteinrikt og får i seg de daglige ca. 1,8 gram av høykvalitetsprotein pr. kg. kroppsvekt som vektrenende anbefales, er det ingen egentlig grunn til å bruke pengene sine på BCAA-tilskudd. La oss se på de studiene som har testet effekten av BCAA og leucin under vekttrening. 4 gram leucin daglig har i ett forsøk vist en gunstig effekt på muskelstyrken (13). Studiet var imidlertid utført på utrente menn, som underveis inntok et kosthold som kun ga en daglig proteinmengde på 0,9 gram pr. kg kroppsvekt. Studiet sier altså ingenting om effekten av leucintilskudd på veltrente personer med et høyt proteininntak. Andre studier på både utrente og svært veltrente personer som er vant til vekttrening viser dessuten at tilskudd med leucin og BCAA ikke egentlig utgjør noen forskjell når man allerede spiser proteinrikt (14 - 16). Forsøk har dessuten vist at myseprotein fungerer like godt som leucin, og kanskje enda bedre, til å stimulere muskelproteinsyntesen (17, 18). Dette kan skyldes at myseproteinpulver både er rikt på leucin, og samtidig også leverer de resterende essensielle aminosyrene som jo fungerer som byggeklosser i proteinsyntesen.  "Flere forsøk har vist at tilskudd med BCAA kan redusere graden av DOMS" "Flere forsøk har vist at tilskudd med BCAA kan redusere graden av DOMS"
 BCAA og DOMS Flere forsøk har vist at tilskudd med BCAA kan redusere graden av DOMS samt blodets innhold av markører for muskelødeleggelse etter både vekttrening (19 - 26) og utholdenhetstrening (27 - 31). Effekten av leucintilskudd i forbindelse med styrketrening er også undersøkt, og her har ett forsøk vist at leucin ikke reduserer markører for DOMS (32), mens et annet studie har vist at tilskudd med leucin i motsetning til hva man ville forvente, faktisk øker DOMS-følelsen (33). Studiene viser imidlertid kun at BCAA er bedre enn uvirksomt placebo. Det vil vi at vi ikke vet om BCAA også er bedre enn vanlig myseprotein eller bare et helt vanlig proteinrikt måltid før og etter trening. Studiene har dessuten blitt utført på fastende deltagere, og dermed vet vi ikke om samme DOMS-reduserende effekt oppnås hvis man har spist et proteinholdig måltid et par timer før trening. Studiene antyder imidlertid at bruk av BCAA kan være berettiget hvis man trener på tom mage (fastende), f.eks. hvis man følger leangains-prinsippene. Er BCAA-tilskudd relevant under et cut? Formålet med et cut er å få skrelt mest mulig fett av kroppen samtidig som tapet av muskelmasse minimeres. Her er det ingen tvil om at det å få i seg tilstrekkelig med protein og essensielle aminosyrer er helt avgjørende. Det er også klart at musklene skal fores med tilstrekkelige mengder BCAA og særlig leucin for å minske muskeltapet mest mulig (12, 34, 35) Nettopp pga. de anabole og anti-katabole effektene av BCAA kunne man forestille seg at tilskuddet er relevant under et cut. Tilskudd med BCAA har riktignok vist gunstige effekter på fettapet under en diett (36), men jeg føler meg ganske overbevist om at BCAA-tilskudd er overflødig hvis man i forveien har økt proteininntaket sitt til > 2 gram pr. kg. kroppsvekt pr. dag, slik det anbefales under et cut. Man kan imidlertid godt argumentere for at BCAA er en kalorisparende måte å få de aller mest anabole aminosyrene på, og nettopp dette kan være relevant for noen idrettsutøvere. Men samtidig skal man huske at pulver, piller og tabletter ikke metter like godt som fast føde i form av kjøtt, fisk og egg.
 Musklene må fores med tilstrekkelige mengder BCAA og særlig leucin for å minske muskeltapet mest mulig Musklene må fores med tilstrekkelige mengder BCAA og særlig leucin for å minske muskeltapet mest mulig
 Bivirkninger og sikkerhet Tilskudd med BCAA ser ut til å være trygt, og man har ikke funnet noen negative effekter ved akutt inntak av 10 – 30 gram (2). For leucin er det blitt fastsatt en øvre daglig grense for inntak på 500 milligram pr. kg kroppsvekt (37, 38). Konklusjon De tre forgrenede aminosyrene leucin, isoleucin og valin, som utgjør BCAA, er viktige essensielle aminosyrer. BCAA stimulerer proteinsyntesen og hemmer nedbrytningen av muskelprotein. Tilskudd med BCAA er imidlertid overflødig hvis man allerede spiser proteinrikt (ca. 1,8 gram protein pr. kg kroppsvekt pr. dag). Vi må nemlig huske på at de gode kildene til kvalitetsprotein; kjøtt, fisk, egg og meieriprodukter, inkludert vanlig myseproteinpulver, er rike på BCAA og særlig leucin. Både under bulk og cut inntar de fleste rikelig med protein, og derfor vil mer BCAA i form av et tilskudd, altså ikke utgjøre noen forskjell. Tilskudd med BCAA kan imidlertid være berettiget under visse omstendigheter. Eksempler på dette er trening i fastende tilstand, eller hvis man vil spare kalorier under en svært kalorirestriktiv cut-periode. Referanser - Mero (1999). Leucine supplementation and intensive training, Sports Medicine, 27: 347 – 58.
- Gleeson (2005). Interrelationship between physical activity and branched-chain amino acids, The Journal of Nutrition, 135: 1591S – 1595S.
- Tom & Nair (2006). Assessment of branched-chain amino acid status and potential biomarkers, The Journal of Nutrition, 136: 324S – 330S.
- Fujita & Volpi (2006). Amino acids and muscle loss with aging, The Journal of Nutrition, 136: 277S – 280S.
- Zanchi et al. (2008). Potential antiproteolytic effects of L-leucine: observations on in vitro and in vivo studies, Nutrition & Metabolism, 17: 20.
- Jefferson & Kimball (2003). Amino acids as regulators of gene expression at the level of mRNA translation, The Journal of Nutrition, 133: 2046S – 2051S.
- Kimball & Jefferson (2004). Amino acids as regulators of gene expression, Nutrition & Metabolism, 1: 3.
- Nair & Short (2005). Hormonal and signaling role of branched-chain amino acids, The Journal of Nutrition, 135, 1547S-52S.
- Shimomura et al. (2004). Exercise promotes BCAA catabolism: effects of BCAA supplementation on skeletal muscle during exercise, The Journal of Nutrition, 134: 1583S – 1587S.
- Apró & Blomstrand (2010). Influence of supplementation with branched-chain amino acids in combination with resistance exercise on p70S6 kinase phosphorylation in resting and exercising human skeletal muscle, Acta Physiologica, 200: 237 – 248.
- Borgenvik et al. (2012). Intake of branched-chain amino acids influences the levels of MAFbx mRNA and MuRF-1 total protein in resting and exercising human muscle, American Journal of Physiology. Endocrinology and Metabalism, 302: 510 – 521.
- Li et al. (2011). Leucine nutrition in animals and humans: mTOR signaling and beyond, Amino Acids, 41: 1185 – 1193.
- Ispoglou et al. (2011). Daily L-leucine supplementation in novice trainees during a 12-week weight training program, International Journal of Sports Physiology and Performance, 6: 38 – 50.
- Spillane et al. (2012). The effects of 8 weeks of heavy resistance training and branched-chain amino acid supplementation on body composition and muscle performance, Nutrition and Health, 21: 263 – 273.
- Herda et al. (2013). Muscle performance, size, and safety responses after eight weeks of resistance training and protein supplementation: a randomized, double-blinded, placebo-controlled clinical trial, Journal of Strength and Conditioning Research, 27: 3091 – 3100.
- Kerksick et al. (2006). The effects of protein and amino acid supplementation on performance and training adaptations during ten weeks of resistance training, Journal of Strength and Conditioning Research, 20: 643 – 653.
- Churchward-Venne et al. (2012). Supplementation of a suboptimal protein dose with leucine or essential amino acids: effects on myofibrillar protein synthesis at rest and following resistance exercise in men, The Journal of Physiology, 590: 2751 – 2765.
- Churchward-Venne et al. (2014). Leucine supplementation of a low-protein mixed macronutrient beverage enhances myofribrillar protein synthesis in young men: a double-blind, randomized trial, The American Journal of Clinical Nutrition, 99: 276 – 286.
- Shimomura et al. (2006). Nutraceutical effects of branched-chain amino acids on skeletal muscle, The Journal of Nutrition, 136: 529S – 532S.
- Shimomura et al. (2010). Branched-chain amino acid supplementation before squat exercise and delayed-onset muscle soreness, International Journal of Sport Nutrition and Exercise Metabolism, 20: 236 – 244.
- Jackman et al. (2010). Branched-chain amino acid ingestion can ameliorate soreness from eccentric exercise, Medicine and Science in Sports and Exercise, 42: 962 – 970.
- Sharp & Pearson (2010). Amino acid supplements and recovery from high-intensity resistance training, Journal of Strength and Conditioning Research, 24: 1125 – 1130.
- Howatson et al. (2012). Exercise-induced muscle damage is reduced in resistance-trained males by branched chain amino acids: a randomized, double-blind, placebo-controlled study, Journal of the International Society of Sports Nutrition, 9: 20.
- da Luz et al. (2011). Potential therapeutic effects of branched-chain amino acids supplementation on resistance exercise-based muscle damage in humans, Journal of the International Society of Sports Nutrition, 8: 23.
- Ra et al. (2013). Combined effect of branched-chain amino acids and taurine supplementation on delayed muscle soreness and muscle damage in high-intensity eccentric exercise, Journal of the International Society of Sports Nutrition, 10: 51.
- Leahy & Pintauro (2013). Branched-chain amino acid plus glucose supplement reduces exercise-induced delayed onset muscle soreness in college-age females, ISRN Nutrition, Mar 17.
- Coombes & McNaughton (2000). Effects of branched-chain amino acid supplementation on serum creatine kinase and lactate dehydrogenase after prolonged exercise, The Journal of Sports Medicine and Physical Fitness, 40: 240 – 246.
- Greer et al. (2007). Branched-chain amino acid supplementation and indicators of muscle damage after endurance exercise, International Journal of Sport Nutrition and Exercise Metabolism, 17: 595 – 607.
- Nosaka et al. (2006). Effects of amino acid supplementation on muscle soreness and damage, International Journal of Sport Nutrition and Exercise Metabolism, 16: 620 – 635.
- Koba et al. (2007). Branched-chain amino acids supplementation attenuates the accumulation of blood lactate dehydrogenase during distance running, The Journal of Sports Medicine and Physical Fitness, 47: 316 – 322.
- Matsumoto et al. (2009). Branched-chain amino acid supplementation attenuates muscle soreness, muscle damage and inflammation during an intensive training program, The Journal of Sports Medicine and Physical Fitness, 49: 424 – 431 (abstract).
- Stock et al. (2010). The effects of adding leucine to pre and postexercise carbohydrate beverages on acute muscle recovery from resistance training, J Strength Cond Res, 24: 2211 – 2219.
- Kirby et al. (2012). Effect of leucine supplementation on indices of muscle damage following drop jumps and resistance exercise, Amino Acids, 42: 1987 – 1996.
- Layman et al. (2003). The role of leucine in weight loss diets and glucose homeostasis, The Journal of Nutrition, 133: 261S – 267S.
- Jitomir & Willoughby (2008). Leucine for retention of lean mass on a hypocaloric diet, Journal of Medicinal Food, 11: 606 – 609.
- Mourier et al. (1997). Combined effects of caloric restriction and branched-chain amino acid supplementation on body composition and exercise performance in elite wrestlers, International Journal of Sports Medicine, 18: 47 – 55.
- Cynober et al. (2012). A proposal for an upper limit of leucine safe intake in healthy adults, The Journal of Nutrition, 142: 2249S – 2250S.
- Elango et al. (2012). Determination of the tolerable upper intake level of leucine in acute dietary studies in young men, The American Journal of Clinical Nutrition, 96: 759 – 767.
|




































